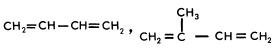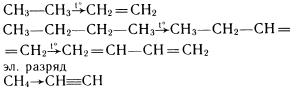Ненасыщенные углеводороды
Непредельные, ненасыщенные углеводороды — большая группа углеводородов, в молекулах которых два или несколько атомов углерода связаны между собой кратными связями (двойными или тройными). К ним относятся: алкены, или олефины, простейший представитель — этилен CH2=CH2, общая формула CnH2n; алкины, или ацетиленовые углеводороды, простейший представитель — ацетилен CH≡CH, общая формула CnH2n-2; алкадиены, алкатриены и другие вещества высокой ненасыщенности. Наиболее подробно изучены алкадиены-1,3, часто называемые сопряженными диенами, дивинил и изопрен:
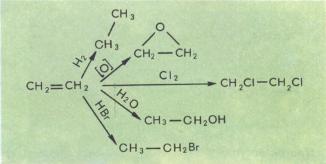
Непредельные углеводороды склонны присоединять водород, кислород, галогены, воду, галогеноводородные кислоты и другие реагенты. Например:
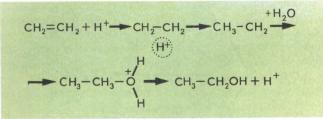
Для активации многих реакций используют катализаторы. Так, присоединение водорода — гидрирование — ускоряется никелем, платиной и другими металлами, адсорбирующими на своей поверхности реагенты (см. Сорбционные процессы). В процессе адсорбции реагенты активируются, что и ускоряет реакцию. Присоединение полярных реагентов (см. Химическая связь), например воды, — гидратация — ускоряется сильными кислотами. Роль таких катализаторов иная. Их протоны образуют комплексы с углеводородами за счет их π-электронов. Такие комплексы в химическом отношении очень активны и легко взаимодействуют с донорами электронов, в данном случае — с атомами кислорода в молекулах воды:
<addc>G</addc>
Протон вступил в первую стадию реакции и выделился в неизменном виде после окончания последней стадии. Такой цикл может повторяться множество раз.
К процессам присоединения относится и полимеризация непредельных углеводородов. Алкены образуют высокомолекулярные насыщенные углеводороды, сопряженные диены — частично ненасыщенные (каучуки, см. Каучуки и эластомеры):
Эти реакции также ускоряются специальными катализаторами.
Непредельные углеводороды могут вступать и в реакции замещения, широко используемые в лабораторной практике и в промышленности. Например, пропилен при высокой температуре хлорируется по месту метильной группы:
Ацетилен и алкилацетилен замещают атом водорода при тройной связи на металл:
2R−C≡C−H + 2Na → 2R−C≡C−Na + H2↑
Реакция объясняется повышенной активностью этих углеводородов в звене ≡C—H.
Для химического синтеза непредельных углеводородов используются разные реакции, среди них все большее значение приобретают термические и каталитические процессы дегидрирования: