Инертные газы
В 1962 г. на страницах химических журналов появились формулы необычных химических соединений: XePtF6, XeF2, XeF4, XeF6. Появление этих веществ было неожиданным потому, что прежде никому в мире не удалось приготовить ни одного химического соединения инертных газов. Так называется совокупность химических элементов, располагающихся на правом «фланге» периодической системы: гелий, неон, аргон, криптон, ксенон, радон.
Способность инертных газов вступать в химические взаимодействия стала второй неожиданностью в их истории. Первая же состояла в самом факте их открытия, которое произошло в течение очень короткого времени — с 1894 по 1898 г. Состав земной атмосферы уже тогда считался хорошо изученным, и не было даже предположений о том, что она может содержать неизвестные газы элементарной природы.
Английский физик Дж. Рэлей обратил внимание на загадочное обстоятельство: плотности атмосферного азота и азота, полученного из химических соединений, различались. Пусть немного, но всегда на одну и ту же величину. Чтобы объяснить эту аномалию, Рэлей обратился за помощью к своему соотечественнику — химику и физику У. Рамзаю. Обсудив ситуацию и повторив эксперименты, ученые пришли к выводу, что в атмосферном азоте содержится примесь неизвестного газа. Его удалось выделить и определить спектр этого газа. Новый газ получил название «аргон», что в переводе с греческого означает «недеятельный», потому что аргон действительно оказался не способным вступать в химические реакции. Некоторое время его даже считали не химическим элементом, а аллотропным видоизменением (см. Аллотропия) азота (подобно тому, как известны кислород O2 и озон O3).
В 1895 г. из уранового минерала клевеита был выделен другой «бездеятельный элемент» — гелий (еще раньше его нашли по спектральным линиям на Солнце и в вулканических газах (см. Спектральный анализ), позднее его обнаружили и в земной атмосфере), а спустя 3 года из воздуха были выделены 3 инертных элемента — криптон, неон и ксенон (названия происходят от греческих слов, означающих соответственно «скрытый», «новый», «чуждый»). Решающая роль в этих открытиях принадлежит У. Рамзаю. Выделить перечисленные газы помогла техника сжижения воздуха и разделения его на фракции, различающиеся по температурам сжижения. Наконец, в 1899 г. в Канаде Э. Резерфорд и Р. Оуэне, изучая явление радиоактивности, доказали существование последнего инертного газа — радона (название от элемента радия, продуктом радиоактивного распада которого является радон).
Некоторое время ученые спорили о том, как разместить инертные газы в периодической системе: ни в одной из ее 8 групп подходящего места не было. В конце концов в 1900 г. пришли к выводу, что целесообразно создать в периодической системе самостоятельную нулевую группу. С тех пор такая группа, включающая элементы с порядковыми номерами 2, 10, 18, 36, 54, 86, стала фигурировать в таблице Менделеева, инертные газы завершали её периоды (с первого по шестой).
Объяснить химическую бездеятельность инертных газов удалось только после разработки планетарной модели атома. Атомы всех инертных газов, кроме гелия, содержат на внешней электронной оболочке 8 электронов. Такой электронный «октет» считался весьма устойчивым, и это представление легло в основу объяснения ионной и ковалентной химической связи (см. Химическая связь). Только в начале 60-х гг. XX в. оказалось, что неспособность инертных газов вступать в химические реакции — заблуждение ученых. Разрушить «броню неприступности» этих элементов помог неметалл - фтор.
Сегодня известно уже около 200 химических соединений ксенона, криптона и радона - фторидов, хлоридов, оксидов, кислот, солей и нитридов. Такое изобилие привело к тому, что в современной периодической системе нулевая группа упразднена: все инертные газы стали помещать в главную подгруппу VIII группы. Правда, с таким решением согласны не все химики: ведь для аргона получение сколь-либо устойчивых химических соединений проблематично, а для гелия и неона оно вообще едва ли возможно.
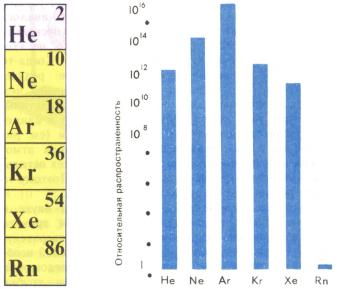
Но и само понятие «инертные», конечно, утратило свой прежний смысл. Нередко гелий и его аналоги называют также благородными газами (поскольку они, как ранее благородный металл золото, не «хотели» вступать в химические реакции). Когда-то У. Рамзай предлагал еще одно название: редкие. Он писал, что «ксенона в воздухе меньше, чем золота в морской воде», и был недалек от истины. Инертные газы действительно принадлежат к наименее распространенным на Земле элементам. Наиболее «богата» земная атмосфера аргоном (его гораздо больше, чем всех остальных инертных газов, вместе взятых). Поэтому-то аргон и был открыт первым.
Инертные газы широко используются в науке и технике. Изучение свойств жидкого гелия привело к удивительным открытиям в физике (сверхтекучести, сверхпроводимости); газообразный гелий необходим для проведения многих научных исследований. Инертными газами заполняют светильники, трубки реклам, лампы различного назначения. Инертные газы используются в производстве сильно окисляющихся веществ. Химические соединения инертных газов также интересны не только для теоретиков; они сильнейшие окислители и поэтому позволили осуществить некоторые казавшиеся ранее необычными химические реакции, например получение соединений пятивалентного золота.